什么是协调标准
欧盟法规 2022-10-24制造商、其他经济运营商或合格评定机构可使用协调标准来证明产品、服务或工艺符合相关的欧盟法规。标准是包含技术信息以一致方式指导或定义实践的已发布文件,医疗器械法规下的协调欧洲标准由欧洲标准化组织根据EC按法规(EU)1025/2012发布的标准化请求制定。协调标准是由欧盟委员会授权的标准化机构制定的标准,符合协调标准要求的产品受益于符合相应基本要求的假设。... 阅读全文
CE-MDR 欧盟 CE 认证 ISO 13485 医疗器械
CE 认证 | MDR 代码的用途/分类/应用
欧盟法规 2022-07-28随着 MDR 的正式实施,各医疗器械制造商已开始逐步提交 MDR 申请,但是在提交过程中难免遇到不少 MDR code。 很多客户表示:对于纷繁复杂的 MDR code 很是陌生和无措。 那么,究竟该如何精确理解并选择 MDR code ?本文将从用途、分类和应用逐一做深度解析。... 阅读全文
CE-MDR 欧盟 CE 认证 欧盟法规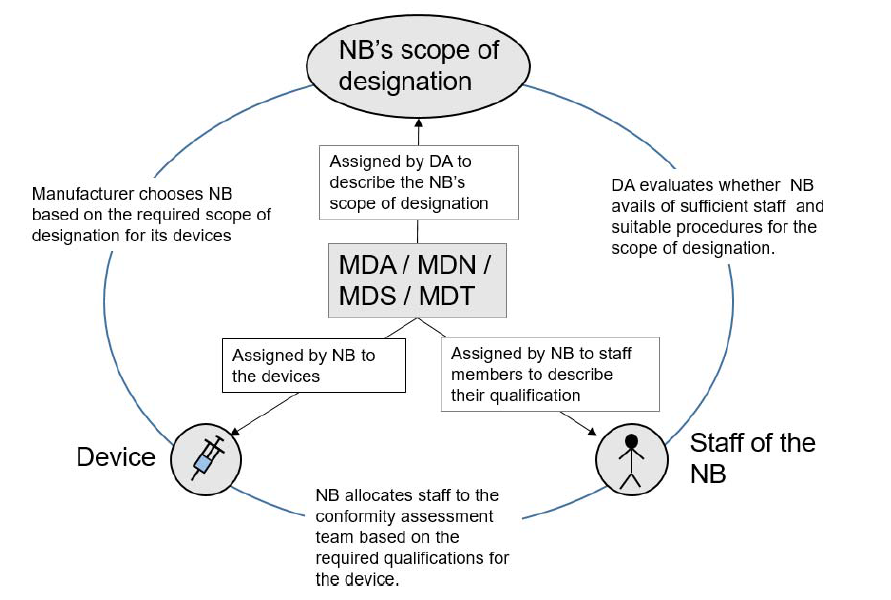
欧盟 MDR 风险管理要求与 ISO 14971:2019 的差异分析
欧盟法规 2022-07-28随着2019年ISO14971和相关技术报告(ISO/TR24971:2020)的发布,已经有很多关于该版本标准与前一版ISO标准(ISO14971:2007)和欧盟协调标准(ENISO14971:2012)要求的比较分析。此前没看到多少关于ISO14971:2019和MDR之间差异的分析。但因为ISO14971:2019在今年5月已成为MDR协调标准,所以这里将尝试做做分析。其他差异:... 阅读全文
CE-MDR 欧盟 CE 认证 欧盟法规
欧盟医疗器械法规MDR正式执行,这些变化需关注
欧盟法规 2022-01-19国产医药器械厂商在申请CE认证时需要注意的点有哪些?医疗器械厂商可以自主选择以旧指令MDD或新法规MDR申请CE证书;如果要申请欧盟认证则必须遵从新规MDR执行。即便是一些电商平台上进行销售的医用产品也需要通过严格的授权公告机构(NotifiedBody,也让目前获批的能够进行新规公告的机构数量大幅降低。医疗器械厂商应在其组织架构内至少配备一名负责监管合规的人员。... 阅读全文
CE-MDR 欧盟 CE 认证
欧盟医疗器械MDR法规认证途径介绍
欧盟法规 2021-12-17在欧盟市场“CE”标志属强制性认证标志,不论是欧盟内部企业生产的产品,还是其他国家生产的产品,要想在欧盟市场上自由流通,就必须加贴“CE”标志,以表明产品符合欧盟《技术协调与标准化新方法》指令的基本要求。这是欧盟法律对产品提出的一种强制性要求。... 阅读全文
CE-MDR ISO 13485 医疗器械
EMDN是什么?EMDE Code的作用有哪些?
欧盟法规 2021-12-14EMDN的全称是European Medical Device Nomenclature,是欧盟委员会于2021年5月4日在CND的基础上发布的欧洲医疗器械命名系统。 根据MDR法规(EU)2017/745第26条和IVDR法规(EU)2017/746第23条,欧洲医疗器械命名法(EMDN)为欧洲医疗器械数据库(EUDAMED)提供支持。... 阅读全文
CE-MDD CE-MDR CE-IVDR 医疗器械 欧盟法规
MDR/IVDR新法规中的各类代码你都清楚了吗?
欧盟法规 2021-06-25每个制造商、欧盟代表、进口商都需要在Eudamed数据库里有这个唯一性识别码,SRN是是明确识别欧盟经济运营商的一种代码。SRN的具体申请手续以及欧盟境外企业申请SRN时的信息核对方法,制造商在递交CE认证申请时需要提供认证产品的Basic UDI-DI。... 阅读全文
CE-MDR 欧盟 CE 认证 CE-IVDR UDI 唯一器械标识 SRN 单一注册号
有关 CE MDR 认证的常见问题解答
欧盟法规 2020-11-09欧盟官方正式发布欧盟医疗器械法规MDR。制造商应逐步更新技术文件以满足MDR法规要求。未取得MDR发证资质的NB将不能签发任何医疗器械CE证书。是否可以延期符合MDR法规要求? 制造商需建立文件化的MDR合规时间表/计划,I类(无菌或测量)器械是否需公告机构介入,但公告机构的审核范围仅限于此类器械无菌和计量方面的内容。MDR法规Art.10所规定的所有一般性义务适用于所有制造商。... 阅读全文
CE-MDR 欧盟 CE 认证
CE认证医疗器械法规MDR更新要点
欧盟法规 2020-01-10但功能和风险与医疗器械类似的产品也纳入MDR(但不含纹身机等),10、MDD/AIMD中的Annex 的临床评估或警戒系统纳入到了MDR的正文里, --- 由医疗机构或外部加工方进行的一次性MD的再加工和再使用必须要符合通用技术规范或协调标准或成员国的法规要求; --- 再加工器械的安全和性能应等同于初期的一次性MD... 阅读全文
CE-MDR 欧盟 CE 认证

