欧盟医疗器械MDR法规认证途径介绍
2021-12-17
“CE”标志是一种安全认证标志,在欧洲市场被视为制造商打开并进入欧洲市场的护照。CE代表欧洲统一(CONFORMITE EUROPEENNE)。

在欧盟市场“CE”标志属强制性认证标志,不论是欧盟内部企业生产的产品,还是其他国家生产的产品,要想在欧盟市场上自由流通,就必须加贴“CE”标志,以表明产品符合欧盟《技术协调与标准化新方法》指令的基本要求。这是欧盟法律对产品提出的一种强制性要求。
在欧盟的法规中,所有商品被分为很多大类,即为下图所示:

其中Regulation (EU) 2017/745 on medical devices 即为欧盟医疗器械的最新法规,简称MDR。
MDR法规把产品根据风险等级的不同,由低到高分为:
I类:基本无风险产品(医用手套、医用口罩、轮椅、病床等)
其中I类产品又分为Is:一类灭菌产品、Ir:一类可重复使用产品、Im:一类测量产品
IIa类:低风险产品(水胶体敷料、气管导管、输液泵的注射筒等)
IIb类:中风险产品(血液透析浓缩、慢性溃疡伤口敷料、拟长期使用的导尿管等)
III类:高风险产品(心血管导管、支架输送导管/系统、神经内窥镜等)
以上分类中,又分为两种途径进行CE认证:
第一种,普通I类产品编写自我符合声明(DOC)。
普通I类医疗器械进行相关的产品测试后并取得测试报告,根据法规要求编写符合标准的技术文件后,交由欧盟授权代表进行注册后,即可完成CE认证,您的产品即可印上"CE"标识以及欧盟授权代表标识。

第二种,Is、Ir、Im、IIa、IIb、III,公告机构审核后发CE证书。
这些分类的产品,因为有一定程度的风险,所以产品的技术资料需要公告机构(NotifiedBody)审核。
欧盟各成员国政府从本国原本存在的第三方认证机构中选择若干具有良好资质的机构,审查后报告给欧盟委员会。欧盟委员会从各成员国上报的名单中选择出若干机构,再次审查,最后确定了一批可以代表欧盟对相关产品实施市场准入审查的机构,分别编号,将名单公告给各成员国,这些机构就叫做第三方“公告机构(Notified Body)简称NB。
每个公告机构都有自己的公告号,截止目前,有MDR公告号的公告机构为:
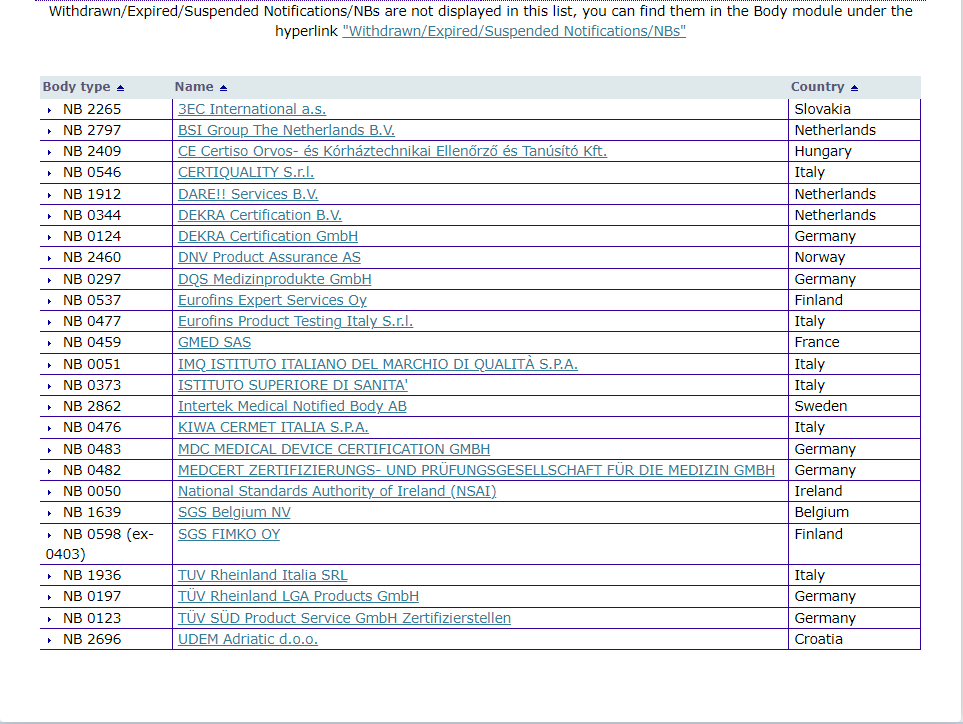
公告机构在审核企业产品技术资料时,技术文件内需要包含企业产品的一系列根据欧盟法规标准所进行的产品测试的合格报告。大部分产品公告机构本身是可以测试并提供报告的。其他测试机构的报告一般要求是有ilac-MRA和CANS标志。部分产品可能需要做临床实验。

另外,公告机构在审核企业产品技术资料时,为了保证企业对产品有良好的质量把控能力,保证审核完成后企业生产的产品能够始终满足标准,并有自我管控能力,还要考察企业的生产现场的ISO13485质量管理体系.
ISO13485中文叫“医疗器械质量管理体系 用于法规的要求” 由于医疗器械是救死扶伤、防病治病的特殊产品,仅按ISO9001标准的通用要求来规范是不够的,为此ISO组织颁布了ISO13485:1996版标准(YY/T0287 和YY/T0288),对医疗器械生产企业的质量管理体系提出了专用要求,为医疗器械的质量达到安全有效起到了很好的促进作用。目前在行的版本为:ISO13485:2016
当企业的ISO13485体系通过认证后,公告机构会给企业颁发ISO13485体系的认证证书:

企业拿到ISO13485证书后,产品的技术部分审核也通过后,即可拿到产品的CE证书:

拿到CE证书后,即可提交欧盟授权代表进行注册。注册完成后就可以在产品上印CE标志和欧盟授权代表标志出口了!
祝各位医疗行业的小伙伴多多出口,开拓国外市场哦!
