国产化大趋势下,如何界定进口医疗器械?
中国法规 2022-08-04政府采购依法对内外资企业在中国境内生产的产品(包括提供的服务,供应链本土化超80%西门子医疗于1992年在上海开设了第一家生产基地”西门子医疗位于上海的实验室诊断试剂工厂也将正式投入使用,届时将成为西门子医疗在亚太地区首家体外诊断试剂研发与生产基地。全球每三台装机的西门子医疗磁共振整机系统中就有一台来自深圳基地。四大全球生产基地GE医疗已经在持续推进全系列、全链条产品的国产创新方面坚持了很多年。... 阅读全文
产品注册许可 进口器械 中国法规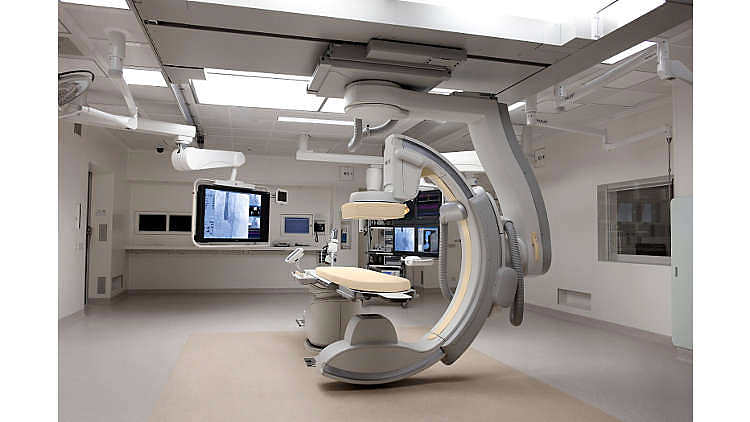
有源医疗器械有效期的评价方法
中国法规 2022-08-02有源医疗器械可实现对疾病的诊断、预防、监护和治疗等功能,为了在临床使用中维持上述功能,医疗器械注册申请人/注册人需确定产品的使用期限。 在该期限内,除了应保证产品安全使用,也应保证产品有效使用。同样,在该期限内,意味着产品采用的所有风险控制措施仍然有效,已知剩余风险依然在可接受范围内。... 阅读全文
医疗器械 中国法规 中国 NMPA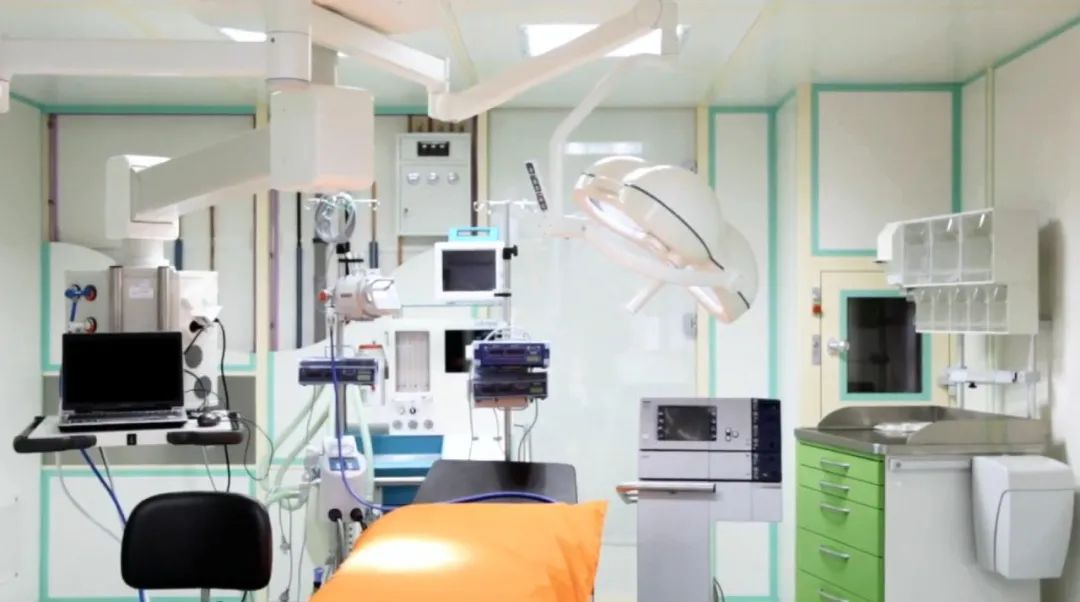
从大量实例深入体会 GMP 法规
中国法规 2022-07-261.4.1技术、生产、质量管理部门负责人应当熟悉医疗器械法律法规,应当有能力对生产管理和质量管理中实际问题作出正确判断和处理;质量管理部质检人员职位任职资格文件(KP3-06-01-R202)规定,对兼职检验员进行监督管理;无产品制造人员具备相应资格或经过针对性的培训记录;设备篇3.2.1生产设备的设计、选型、安装、维修和维护应当符合预定用途;... 阅读全文
典型案例 医疗器械 中国法规 中国 NMPA GMP 体考
进口医疗器械注册申请
中国法规 2022-07-26向国务院食品药品监督管理部门提交注册申请资料和注册申请人所在国(地区)主管部门准许该医疗器械上市销售的证明文件”第二类、第三类医疗器械产品注册申请资料中的产品检验报告应当是医疗器械检验机构出具的检验报告:... 阅读全文
产品注册许可 进口器械 中国法规 中国 NMPA
关于《医疗器械生产许可证》的相关问答
中国法规 2022-07-26《医疗器械生产许可证》是什么?《医疗器械生产许可证》是从事第二类、第三类医疗器械生产活动的企业,《医疗器械生产许可证》有副本吗?《医疗器械生产许可证》分为正本和副本。《医疗器械生产许可证》有效期多长时间?《医疗器械生产许可证》有效期为5年。哪些企业需要申请《医疗器械生产许可证》?从事第二类、第三类医疗器械生产活动的企业,依法取得《医疗器械生产许可证》。申请《医疗器械生产许可证》需要多长时间?... 阅读全文
产品注册许可 医疗器械 中国法规 生产许可证 中国 NMPA
NMPA | 射频美容类器械、灸疗类医疗器械分类界定指导原则
中国法规 2022-07-22射频美容类医疗器械属性界定 符合《医疗器械监督管理条例》有关医疗器械含义的射频美容类产品,达到局部浅表温和加热、改善血液循环等目的的射频美容类产品,(二)预期使用射频能量作用于人体(包括但不限于皮肤组织及皮下深层软组织等),且可能会对人体造成潜在的影响或损伤(如组织即刻收缩反应、组织变性、细胞凋亡等)的射频类美容产品,分类界定 ... 阅读全文
产品注册许可 医疗器械 医用 中国法规 中国 NMPA
新版《医疗器械注册与备案管理办法》最新 FAQ(常见问答)
中国法规 2022-02-16一、关于《办法》实施前后有关第二类医疗器械(含体外诊断试剂)注册申请执行要求1.《办法》实施后,第二类医疗器械注册申请材料应当符合《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2021年第121号)》和《关于公布体外诊断试剂注册申报资料要求和批准证明文件格式的公告(2021年第122号)》的规定。注册人应提交申请延续注册前已获得原审批部门批准的变更注册(备案)文件及其附件的复印件。... 阅读全文
标准解读
关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2021年第121号令)
中国法规 2021-10-09根据《医疗器械监督管理条例》(国务院令第739号)和《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号),国家药监局组织制定了医疗器械注册申报资料要求和批准证明文件格式(见附件),原国家食品药品监督管理总局发布的《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》(原国家食品药品监督管理总局公告2014年第43号)同时废止。... 阅读全文

中国医疗器械唯一标识(UDI)实施释疑
中国法规 2021-06-25由注册人/备案人将唯一标识的产品标识及关联信息按照相关标准和规范上传至数据库,医疗器械经营企业、医疗机构、政府相关部门及公众可通过数据查询、下载、数据对接等方式共享唯一标识数据。在注册/备案管理系统中提交其产品标识。在产品上市销售前应当完成医疗器械唯一标识产品标识和相关数据的上传。《规则》实施之日前已生产、销售的医疗器械可不具备医疗器械唯一标识。... 阅读全文
UDI 唯一器械标识 中国法规 中国 NMPA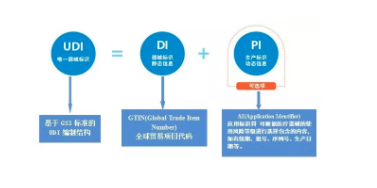
【关注】国家药监局对《医疗器械分类目录》部分内容进行了调整!
中国法规 2021-01-11国家药监局关于调整《医疗器械分类目录》部分内容的公告(2020年 第147号)为进一步深化医疗器械审评审批制度改革,药品监督管理部门依据《医疗器械注册管理办法》《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》《关于第一类医疗器械备案有关事项的公告》等,按照调整后的类别受理医疗器械注册和备案申请。按照改变后的类别向相应药品监督管理部门申请延续注册。... 阅读全文
中国法规
