欧盟医疗器械单一注册号SRN码你申请了吗?
2021-06-25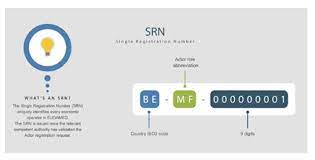
欧洲议会和理事会于2017年4月5日颁布的《医疗器械法规(EU)2017/745》(简称“ MDR”)第33条规定,委员会在咨询MDCG之后,应建立、维护和管理欧洲医疗器械数据库EUDAMED。
2020年12月1日开始,EUDAMED数据库的注册功能模块启用,随着数据库的逐渐上线,将提高欧盟医疗器械市场的透明度和协调性。
相关经济运营商(EO)包括制造商、授权代表、进口商、经销商,都要求使用这个SRN注册模块。
对于企业,在向公告机构申请符合性认证、访问 Eudamed、现场安全通告、安全和临床性能总结、欧盟符合性声明和向 UDI 数据库登记UDI时都需要使用在Eudamed注册后获得的SRN(单一注册号)。
在Eudamed中注册的信息需要在首次注册1年内进行一次准确性确认,且此后每2年需要再确认。信息应按MDR附录VI,最晚需要在Eudamed正式发布或者法规过渡期结束后18个月的过渡期内完成注册。
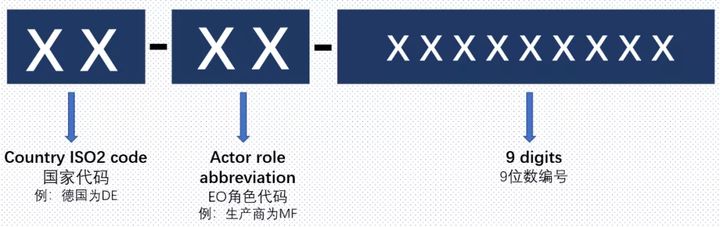
SRN 单一注册号Single Registration Number
按照MDR第30条第1款要求,注册功能模块会生成MDR第32条第2款提及的独一无二的单一注册号(SRN)。
MDR第31条第2款规定,成员国主管当局在核实和确认申请者数据后,会通过Eudamed注册功能模块中获取SRN,并将其提供给制造商、欧代或进口商。一个EO角色对应一个SRN。此外每一个SRN中也会体现该编号对应的角色。
文件需求
A·信息安全责任宣言
所有参与者必须上载已签署的信息安全责任宣言
B·授权摘要文件
要在EUDAMED中进行注册,非欧盟制造商必须拥有有效的授权代表
并随注册一起提交授权摘要文件
注册流程
以企业的经营者为例
01制造商将注册申请递交给授权代表
02授权代表验证注册请求
03授权代表将验证通过的注册申请递交给主管当局
04主管当局对注册申请进行审核评估
05批准注册请求后将由主管当局生成核发登记证明书
Eudamed通过电子邮件将SRN发送给制造商
