事关二三类医械 | 自2022年11月1日起,全面实施医疗器械电子注册证
2022-11-03国家药监局于2020年10月试点发放国产第三类、进口第二、三类医疗器械注册证,并逐步试点发放了与电子注册证关联的注册证变更文件,现已发放医疗器械电子注册证1.4万张、注册证变更文件0.35万张。全面实施医疗器械电子注册证。一、此次医疗器械电子注册证发放范围为自2022年11月1日起,由国家药监局批准的国产第三类、进口第二、三类医疗器械注册证及注册变更文件。... 查看详情

欧盟MDR的NB机构增至34家!20天内连增2家
2022-10-15又新增了一家在MDR法规下的NB机构:已经获得授权的MDR公告机构一共达到了34家。34家MDR法规NB机构清单ENTECERTIFICAZIONEMACCHINESRL这家NB机构来自意大利,该NB机构就可以在欧盟内的医疗器械领域广泛地作为公告机构开展工作。意大利境内的MDR公告机构已经达到了9家,成为欧盟拥有MDR公告机构最多的国家。... 查看详情

202207 | 欧盟更新 MDR 和 IVDR 实施滚动计划
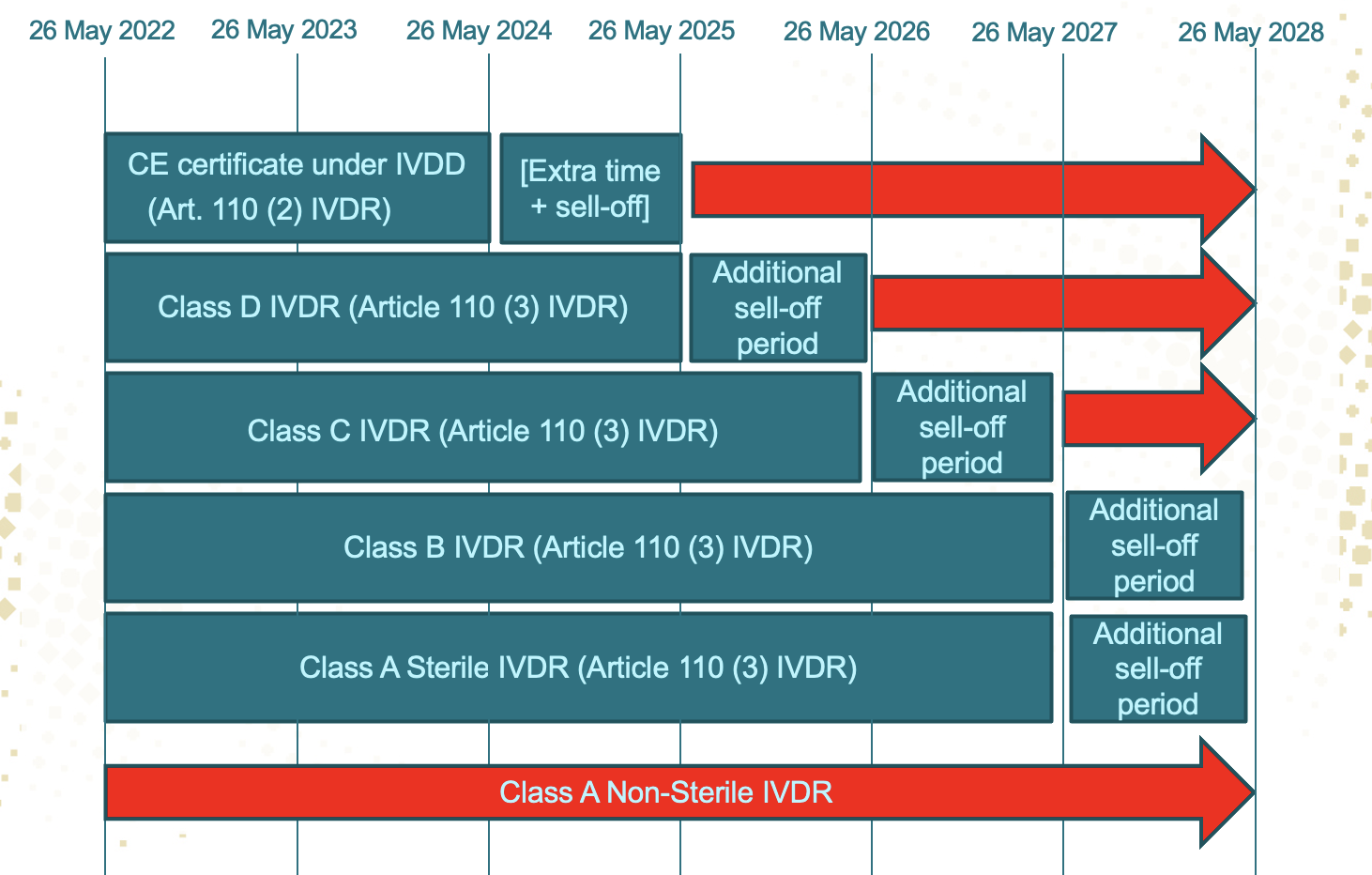
2022-07-28IVDR实施滚动计划”该滚动计划包含委员会已通过或打算在未来通过的已确定的基本实施法案和其他相关举措的清单。实施行为和其他行动/倡议。该文件每季度进行一次审查,以便为国家监管者和利益相关者提供最新信息。2022第三季度的滚动计划中有待完成的项目总结如下:实施计划根据此滚动计划,结合MDCG指南的编制计划,欧盟委员会在逐步完善MDR&IVDR实施。制造商需要根据当局释放的这些法规计划。... 查看详情

输美食品迎重大调整:无邓白氏编码将被拒绝入境!
2022-07-20近日,美国食品药品管理局(FDA)发布了一项重要通知,从2022年7月24日起,如果输美“人或动物食品企业编号”一栏中未提供邓白氏编码,美国海关和边境保护局将拒绝相关企业食品入境。... 查看详情


英国UKCA重大更新:2023-7-1前生效
2022-07-19在2021年9月至2021年11月期间,药品和保健产品监管机构 (MHRA) 就英国 (UK) 医疗器械监管框架的拟议变更进行了咨询英国主管当局(MHRA)计划让新的英国医疗器械法规在2023年7月1日前生效。 MHRA 今年6月26日发布了一咨询回应“Government response to consultation on the future regulation of medical devices in the United Kingdom”,里面除了提示了一些英国新法规可能会出现的内容,与欧洲MDR/IVDR的异同等内容,还提到非常重要的信息,就是MHRA准备为新法规提供转换期,使已经有UKCA或者CE标识的产品,在英国新法规生效后,仍然可以在英国(GB)市场上注册并销售。... 查看详情

eMDR更新 | FDA宣布推出电子医疗器械问题报告系统增强功能
2022-07-112022年7月8日,FDA发布通告,公布了CDRH 的电子医疗器械问题报告 (eMDR) 系统的增强功能。值得注意的是,FDA eSubmitter客户端将与 eMDR 系统同时更新,但具有系统-系统或 AS2 帐户的行业使用FDA 电子提交网关 (ESG)应使用此页面上的信息来计划系统更新以与这些保持一致尽快增强 eMDR 系统。... 查看详情

IVDR确定延期!!
2022-02-081、过渡期总体由 推迟到 2、在2022.5.26之前完成了NB发证的IVDD下ListA,之前完成了IVDD符合性声明(欧盟注册)的,之后完成IVDD符合性声明(欧盟注册)的,2022.5.26 PMS、警戒系统、经济运营商注册这些要求,企业需及时更新QMS,同时依据IVDR要求实施企业注册、产品注册等;6、根据释疑 Q&... 查看详情
FDA更新了口罩和呼吸器的执法政策
2021-12-13美国食品和药物管理局(FDA)更新了最初于2020年4月发布的新冠疫情大流行期间口罩和呼吸器的执法政策。包括对符合政策条件的口罩的通用紧急使用授权(EUA)。该政策免除了对符合条件的产品提交上市前通知(510k)的要求,FDA制定这一政策旨在增加美国的口罩供应,做出此类声明的口罩需要获得FDA批准”FDA还将EUA扩展到某些口罩;以便医疗机构在疫情期间有足够的口罩;... 查看详情

