202208 | FDA 提供机构应对猴痘疫情的最新情况
2022-08-04FDA正在提供其在美国对猴痘的多管齐下应对的最新情况,提供有关FDA正在进行的与猴痘有关的监管活动的重要信息以及常见问题。FDA将随着事态发展提供更新,美国疾病控制和预防中心(CDC)有一项FDA批准的非天花正痘病毒检测,FDA不知道临床数据支持使用其他样本类型(如血液或唾液)进行猴痘病毒检测。FDA批准的猴痘测试由CDC和包括CDC公共卫生实验室响应网络在内的许多实验室提供。... 查看详情

美国 FDA 发布关于猴痘病毒检测的指导文件!
2022-07-20FDA还未获知使用其他样本类型(例如血液或唾液)进行猴痘病毒检测的临床数据。包括临床医生常见问题解答以及为猴痘病毒检测准备和收集的样本。请考虑使用病变拭子样本重新检测您的患者。向FDA报告您在猴痘病毒检测中遇到的任何问题,猴痘测试说明和背景猴痘病毒测试用于确定一个人是否感染了导致猴痘的病毒。CDC经FDA批准的非天花正痘病毒测试可以从病变样本中检测出猴痘。... 查看详情
快讯 | FDA 试点递交文档的新方式
2022-07-20这项工作是 FDA 与业界合作并提高医疗器械审查过程效率的持续承诺的一部分。从长远来看,该递交流程将向所有行业合作伙伴提供,并将取代制作包含 eSTAR 或 eCopy 文件的任何光盘(CD)、数字视频光盘(DVD)或闪存驱动器并将其邮寄给 FDA 的需求。... 查看详情


20220711 | 首款国产新冠特效药上市:万元以内,能走医保
2022-07-11在宣布其长效新冠联合疗法在中国商业化上市后,腾盛博药在近期回应了网友关于这款特效药的疑问:首批药物发往了深圳市第三人民医院,下一步将通过华润药业、上海医药和国药控股三家经销商,分发全国;低于海外同类药物(1500~2000美元),能走医保;产能如何:腾盛博药已与全球生物制药合同开发生产龙头企业药明生物达成合作,可根据全球及国内的防疫需求来匹配产能。... 查看详情

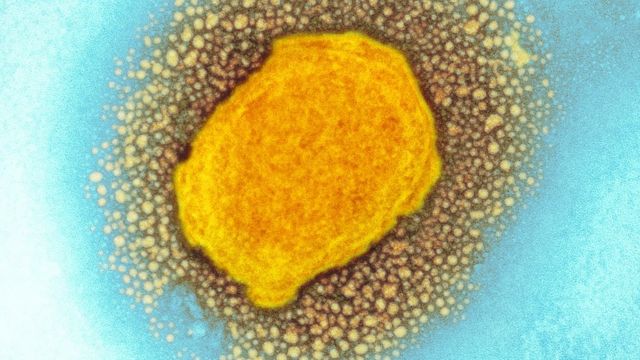
致命病毒恐掀新疫情!致死率高达90%,无疫苗可打!
2022-07-11起初医护人员以为是埃博拉病毒,甚至比埃博拉还可怕的病毒……经过日本野口医学研究所(NoguchiMemorialInstituteforMedicalResearch)从两名患者身上采集的样本分析,第二次在西非爆发马尔堡病毒疫情!加纳的卫生官员们正在紧张地为疫情爆发做准备,感染病毒的患者都会出现类似的出血热症状,当时德国的医疗机构从非洲乌干达采购了一批绿猴用于医学研究。... 查看详情

印度10月后将强制注册,可能会影响很大一批没有进口资质的企业出口
2022-07-11所有剩余的未通知的C类和D类设备都需要获得进口许可证。4-审核流程-所有医疗器械都必须注册或拥有进口许可证。需要进口许可证的产品类型的完整列表可以在本页底部找到。设备类别需要通过提交每个产品的设备主文件(DMF)和每个制造场所的工厂主文件(PMF)来获得进口许可证。医疗器械将根据与主要制造地点相关的进口许可证进行注册。其余未通知的C类和D类设备需要在2023年10月1日之前获得进口许可证。... 查看详情

划重点 | 美国FDA对于医疗器械与药品注册更新的时间规定
2021-12-13美国食品和药物管理局(FDA)要求生产和分销预期在美国使用的医疗器械和药品的企业每年需更新其FDA注册。这些企业必须在2021年10月1日至2021年12月31日之间将其注册更新至2022年。... 查看详情

