速看 | MDR公告机构增至31家
2022-07-19该公告机构是西班牙境内第1家公告机构,公告机构编号:NB 0318。

2022年7月14日,位于西班牙的AGENCIA ESPAÑOLA DE MEDICAMENTOS Y PRODUCTOS SANITARIOS(公告机构编号:NB 0318)获得MDR审核资质,至此MDR公告机构新增到31家。
该公告机构是西班牙境内第1家公告机构。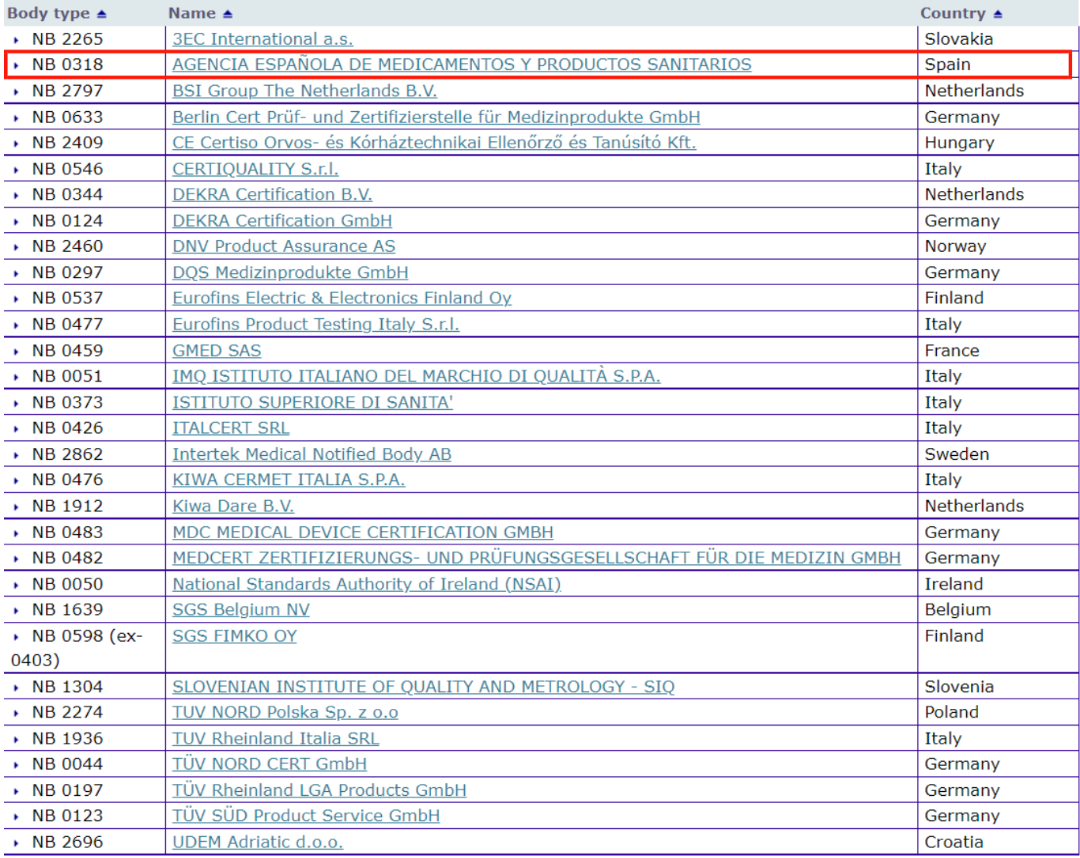
现在共有 38 家公告机构根据欧盟法规工作,其中 7 家是IVDR公告机构。
算上本次新增的MDR公告机构AGENCIA ESPAÑOLA DE MEDICAMENTOS Y PRODUCTOS SANITARIOS,根据欧盟MDR法规工作的31家公告机构的地理分布如下:德国 8 家、意大利 7 家、荷兰 3 家、芬兰 2 家,西班牙、斯洛文尼亚、波兰、比利时、克罗地亚、法国、匈牙利、爱尔兰、挪威、斯洛伐克和瑞典各有一家。
根据IVDR法规工作的7家公告机构位于:德国 3家、荷兰 2家 、法国 1家和斯洛伐克1家。
