IVDR确定延期!!
2022-02-08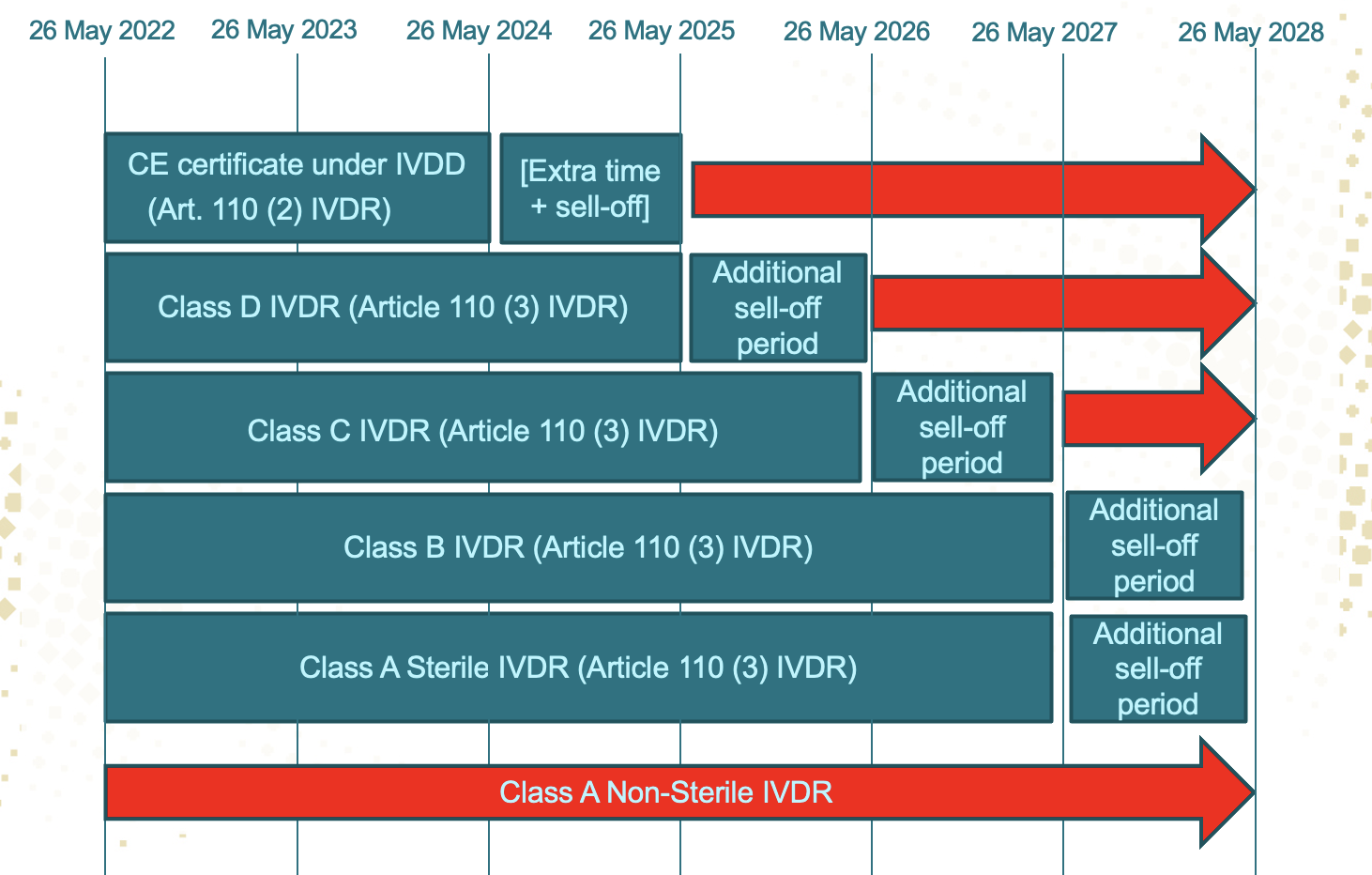
2022年1月25日,欧洲议会和欧盟委员会发布REGULATION (EU) 2022/112,确定了IVDR 过渡期延期事宜。

依据发布的REGULATION (EU) 2022/112,具体延期如下:
1、过渡期总体由 2024.5.27 推迟到 2025.5.27;
2、在2022.5.26之前完成了NB发证的IVDD下List A, List B和Self-test产品,可继续销售至2025.5.26;
3、对于 IVDD 下 other 类产品,在 2022.5.26 之前完成了IVDD符合性声明(欧盟注册)的,在如下日期之前仍可上市销售:
· Class D(IVDR下)2025.5.26;
· Class C(IVDR下)2026.5.26;
· Class B(IVDR下)2027.5.26;
· Class A无菌(IVDR下)2027.5.26。
4、对于 IVDD 下 other 类产品,在 2022.5.26 之后完成IVDD符合性声明(欧盟注册)的,在如下日期之前可上市销售:
· Class D(IVDR下)2026.5.26;
· Class C(IVDR下)2027.5.26;
· Class B(IVDR下)2028.5.26;
· Class A无菌(IVDR下)2028.5.26。
5、IVDR 新政并没有推迟,还是 2022.5.26 实施;PMS、警戒系统、经济运营商注册这些要求,依旧自2022.5.26立即实施;由此,企业需及时更新QMS,同时依据IVDR要求实施企业注册、产品注册等;
6、根据释疑 Q&A ,IVDR 实施后的 Class A(非无菌)产品,由于不需要 NB 介入,所以从 2022.5.26 开始立即全面实施,也就是要按 IVDR 做注册。
